Thomson Atom Modeli ve Rutherford Atom Modeli

- Özgün
Atom Modelinin Tarihsel Gelişimi
MÖ. 5. yüzyılda Demokritos bu soruyu cevaplamaya çalışanlardan biriydi. Demokritos'a göre, madde parçalara ayrıldığında, en sonunda bölünemeyen bir tanecik elde edilir ve bu tanecik atomdur. Bu basit önerme, parçacık fiziğine giden çok uzun ve dolambaçlı yolun yalnızca başlangıcıydı.Demokritos'un önermelerinin ardından günümüz atom modeline giden yolda diğer bir adım, John Dalton tarafından atıldı. John Dalton'un önermelerini 3 başlık altında toplayabiliriz.
- Atomlar, kimyasal tepkimelerle oluşamaz ve alt parçalara bölünemez.
- Bir elementin atomlarının kütlesi ve diğer kimyasal özellikleri aynıdır.
- Kimyasal bileşikler, element atomlarının birleşmesi ile oluşur.
Thomson Atom Modeli
J. J. Thomson, çok kısa bir süre önce William Crookes'un icat ettiği katot ışın tüpleri ile deneyler yapıyordu. Yapılan tüm deneylerde olduğu gibi onun deneylerinde de ışınlar katot (-) uçtan anot (+) uca doğru hareket ediyordu. Thomson bu deneyi biraz geliştirmek istedi ve tüpün sonuna bir floresan ekran koydu. Koyduğu bu floresan ekran sayesinde ışınların yönlenmesini inceleyebilecekti. Katot ışınlarının yüklü olup olmadığını anlamak için ışınların geçtiği yola iki adet zıt yüklü levha koydu ve ışınların bu levhalar arasından geçmesini sağladı. Yaptığı deneyler sırasında ışınların pozitif yüklü levhaya doğru kırıldığını gözlemledi. Bu tek bir sebepten olabilirdi: Işınlar negatif yüklü olmalıydı!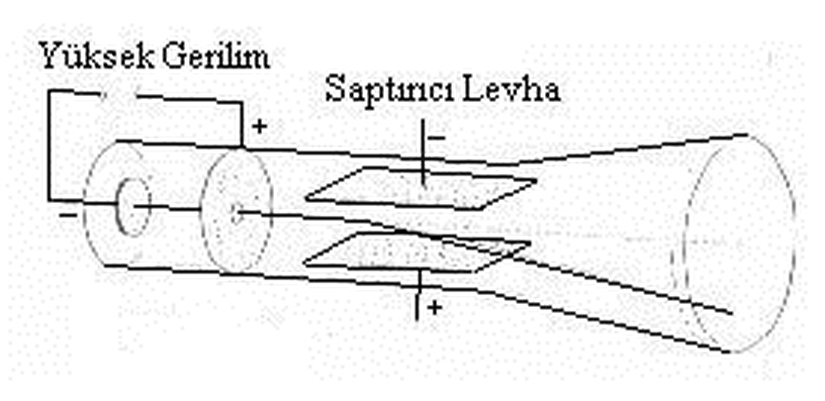
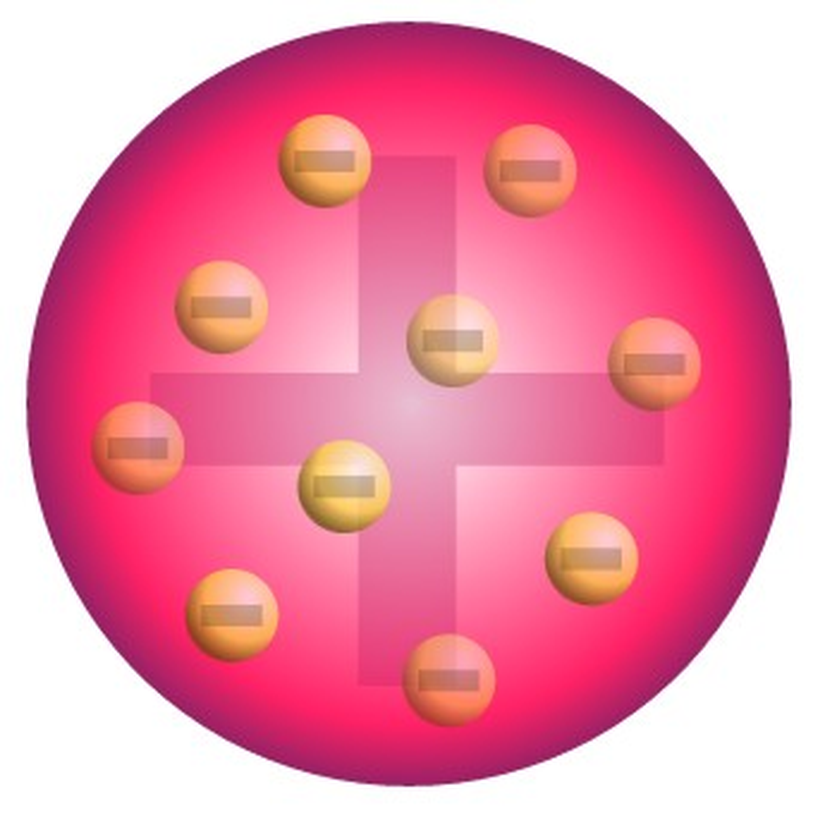
Rutherford Atom Modeli
Thomson atom modeli kusursuz değildi. Thomson'ın öğrencisi Rutherford kontrolünde çalışan Hans Geiger ve Ernest Marsden tarafından yapılan deneyler, Thomson atom modeli ile açıklanamıyordu.Geiger ve Marsden'in yaptığı deney, alfa parçacığı (2 proton + 2 nötron) gönderen bir kaynak ve karşısında da altın bir plakadan oluşuyordu. Plaka, floresan ekran ile çevrelenmişti ve bu sayede plakadan saçılan parçacıkların yöneldiği bölgeler gözlemlenebiliyordu.
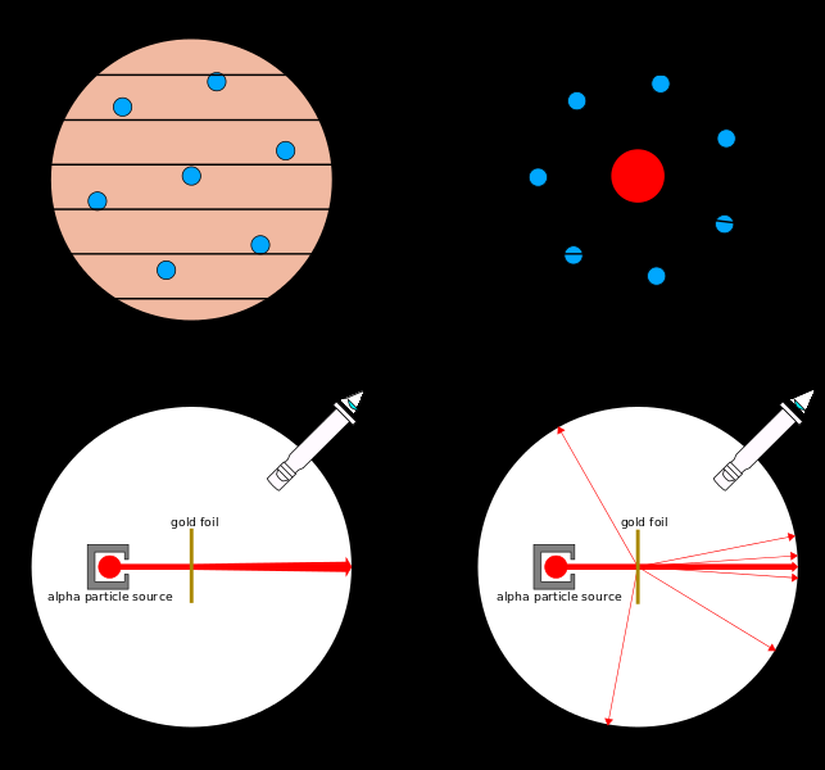
1911 yılında Rutherford'un yaptığı deneylerde bir miktar saçılma gözleniyordu. Bu da tek bir şeye, pozitif yükün çok küçük bir hacimde toplanmış olduğuna işaret ediyordu. Yapmış olduğu deneyler ışığında Rutherford, hocası olan Thomson'ın atom modelini reddetti (boynuz kulağı geçmişti anlaşılan) ve ortaya yeni bir atom modeli attı. Bu model Rutherford atom modeli olarak anılacaktı.
Merkezde çok küçük bir hacimde toplanmış pozitif yük ve etrafında da negatif yükler bulunmaktaydı. Bu büyük bir şeydi çünkü modern atom modeline en benzer yapı, Rutherford atom modeli tarafından ortaya koyulmuştu. Bohr'un geliştirmesi ile devam edecek olan bu süreç, bizim şu an bildiğimiz atom modeline giden çok önemli bir basamaktı.
Modelinde her ne kadar yanlış önermeler varsa da, Thomson atom modeli bize çok önemli bir şey göstermişti. Atom, alt parçacıklar içeriyordu. Öğrencisi Rutherford'un geliştirdiği model ise Bohr'un devrim niteliğindeki çalışmaları ile devam edecek olan uzun yolda adeta bir dönüm noktasıydı. Kuantum fiziğinin temellerinden standart modele kadar her şey, bu iki bilim insanının önermeleri ile ilk adımlarını atmıştı.
Yazan:Ege Can Karanfil
Geliştiren:Deniz Gamze Sanal
Editör: Ögetay Kayalı
Referanslar
- <http://hyperphysics.phy-astr.gsu.edu/hbase/Nuclear/rutsca3.html>
- <https://www.universetoday.com/38326/plum-pudding-model/>
- <https://edtech2.boisestate.edu/lindabennett1/502/thompson.html>
- <http://www.nobelprize.org/nobel_prizes/chemistry/laureates/1908/rutherford-bio.html>
- <http://www.nobelprize.org/nobel_prizes/physics/laureates/1906/thomson-bio.html>
- <http://www.visionlearning.com/en/library/Chemistry/1/Early-Ideas-about-Matter/49>
- <https://en.wikipedia.org/wiki/Geiger%E2%80%93Marsden_experiment#/media/File:Geiger-Marsden_experiment_expectation_and_result.svg>
- <https://www.universetoday.com/38326/plum-pudding-model/>
- <https://tr.wikipedia.org/wiki/Thomson_atom_modeli#/media/File:Thomson%E2%80%99%C4%B1_elektronun_ke%C5%9Ffine_g%C3%B6t%C3%BCren_deney_d%C3%BCzene%C4%9Fi.gif>
İçeriklerimizin bilimsel gerçekleri doğru bir şekilde yansıtması için en üst düzey çabayı gösteriyoruz. Gözünüze doğru gelmeyen bir şey varsa, mümkünse güvenilir kaynaklarınızla birlikte bize ulaşın!
Bu içeriğimizle ilgili bir sorunuz mu var? Buraya tıklayarak sorabilirsiniz.
Soru & Cevap Platformuna Git- 0
- 0
- 0
- 0
- 0
- 0
- 0
- 0
- 0
- 0
- 0
- 0
Evrim Ağacı'na her ay sadece 1 kahve ısmarlayarak destek olmak ister misiniz?
Şu iki siteden birini kullanarak şimdi destek olabilirsiniz:
kreosus.com/evrimagaci | patreon.com/evrimagaci
Çıktı Bilgisi: Bu sayfa, Evrim Ağacı yazdırma aracı kullanılarak 25/04/2024 03:17:12 tarihinde oluşturulmuştur. Evrim Ağacı'ndaki içeriklerin tamamı, birden fazla editör tarafından, durmaksızın elden geçirilmekte, güncellenmekte ve geliştirilmektedir. Dolayısıyla bu çıktının alındığı tarihten sonra yapılan güncellemeleri görmek ve bu içeriğin en güncel halini okumak için lütfen şu adrese gidiniz: https://evrimagaci.org/s/12834
İçerik Kullanım İzinleri: Evrim Ağacı'ndaki yazılı içerikler orijinallerine hiçbir şekilde dokunulmadığı müddetçe izin alınmaksızın paylaşılabilir, kopyalanabilir, yapıştırılabilir, çoğaltılabilir, basılabilir, dağıtılabilir, yayılabilir, alıntılanabilir. Ancak bu içeriklerin hiçbiri izin alınmaksızın değiştirilemez ve değiştirilmiş halleri Evrim Ağacı'na aitmiş gibi sunulamaz. Benzer şekilde, içeriklerin hiçbiri, söz konusu içeriğin açıkça belirtilmiş yazarlarından ve Evrim Ağacı'ndan başkasına aitmiş gibi sunulamaz. Bu sayfa izin alınmaksızın düzenlenemez, Evrim Ağacı logosu, yazar/editör bilgileri ve içeriğin diğer kısımları izin alınmaksızın değiştirilemez veya kaldırılamaz.



